Views 1695
2024-02-16 10:00

(กูรูเช็ค) สรุป! โพรไบโอติก ที่ อย. ไทย อนุญาตใช้พร้อมขั้นตอนการขอใช้โพรไบโอติกตัวใหม่
ปัจจุบันมีการใช้โพรไบโอติกในอาหารและผลิตภัณฑ์อาหารเสริมอย่างแพร่หลาย ดังนั้นเพื่อให้การใช้โพรไบโอติกในอาหารและผลิตภัณฑ์อาหารเสริมเป็นไปอย่างถูกต้องเหมาะสม และปลอดภัยต่อการบริโภค ตามประกาศของสํานักงานคณะกรรมการอาหารและยา กระทรวงสาธารณสุข กูรูเช็คเลยอยากนำเสนอข้อมูลอีกแง่สำหรับผู้ประกอบการอาหารเสริมโพรไบโอติก เพื่อตรวจสอบสายพันธุ์โพรไบโอติกที่ อย. บ้านเราอนุญาตให้ใช้ในอาหารและขั้นตอนการขออนุญาตใช้สายพันธุ์โพรไบโอติกใหม่ที่ผ่านการวิจัย รายละเอียดเป็นยังไงติดตามกันเลยค่ะ
ความหมายของคําว่า “จุลินทรีย์โพรไบโอติก (Probiotic)” ซึ่งสรุปได้ว่า จุลินทรีย์โพรไบโอติก นั้นหมายถึงจุลินทรีย์ที่มีชีวิตซึ่งใช้ในอาหารและจะเกิดผลต่อสุขภาพก็ต่อเมื่อลูกค้าได้รับในปริมาณที่เพียงพอ
กําหนดเงื่อนไขอาหารที่มีการใช้โพรไบโอติกต้องเป็นดังนี้
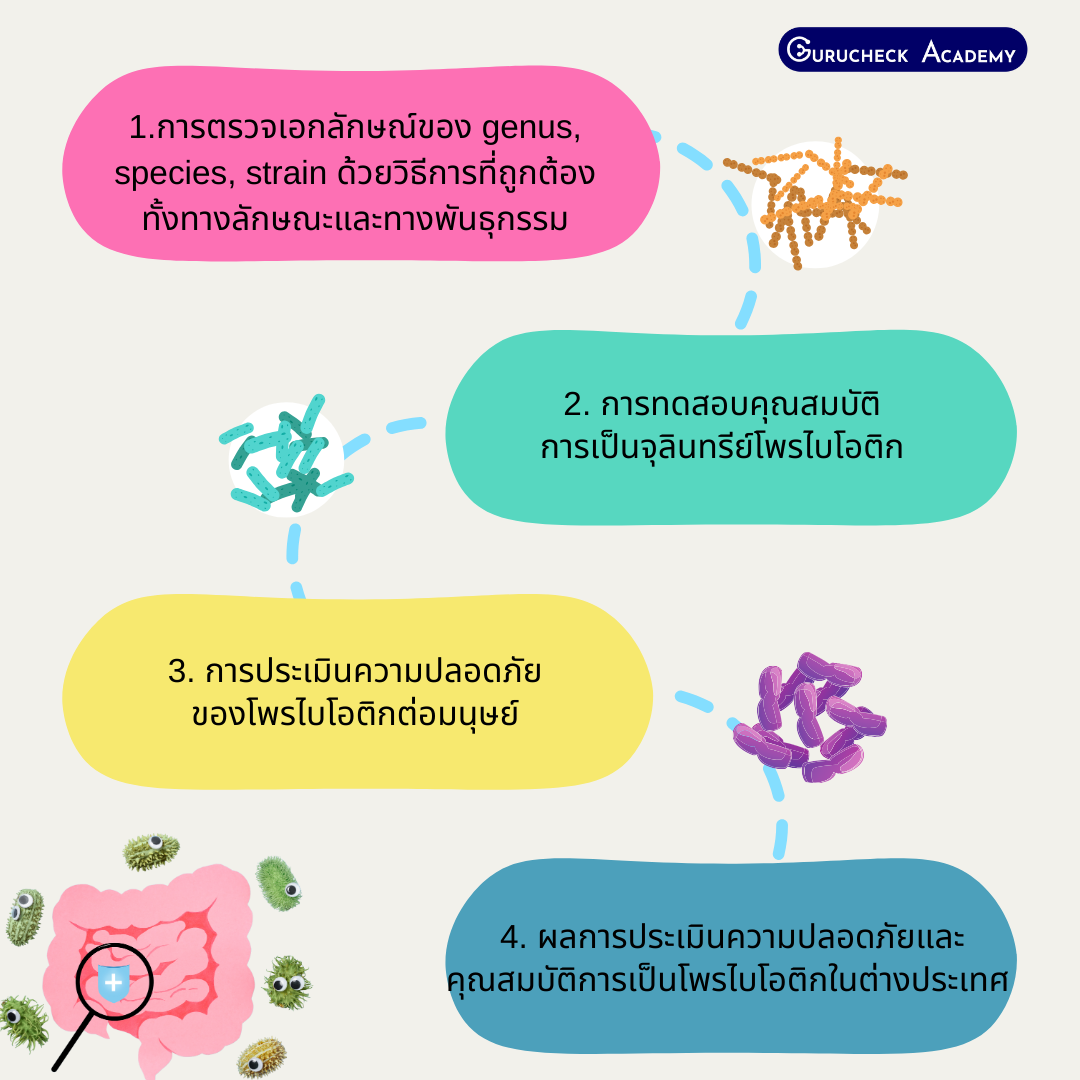
การใช้จุลินทรีย์โพรไบโอติกอื่นนอกเหนือจากที่กำหนดไว้ในบัญชีตามประกาศ อย. ผู้ผลิตหรือผู้นำเข้าต้องส่งหลักฐานแสดงผลการประเมินความปลอดภัย และคุณสมบัติการเป็นโพรไบโอติก ตามหลักการใน Guidelines for the Evaluation of Probiotics in Food, Joint FAO/WHO Working Group Report on Drafting Guidelines for the Evaluation of Probiotics in Food,ปี ค.ศ. 2002 พร้อมรายละเอียดข้อมูลประกอบการยื่นขออนุญาต ดังนี้
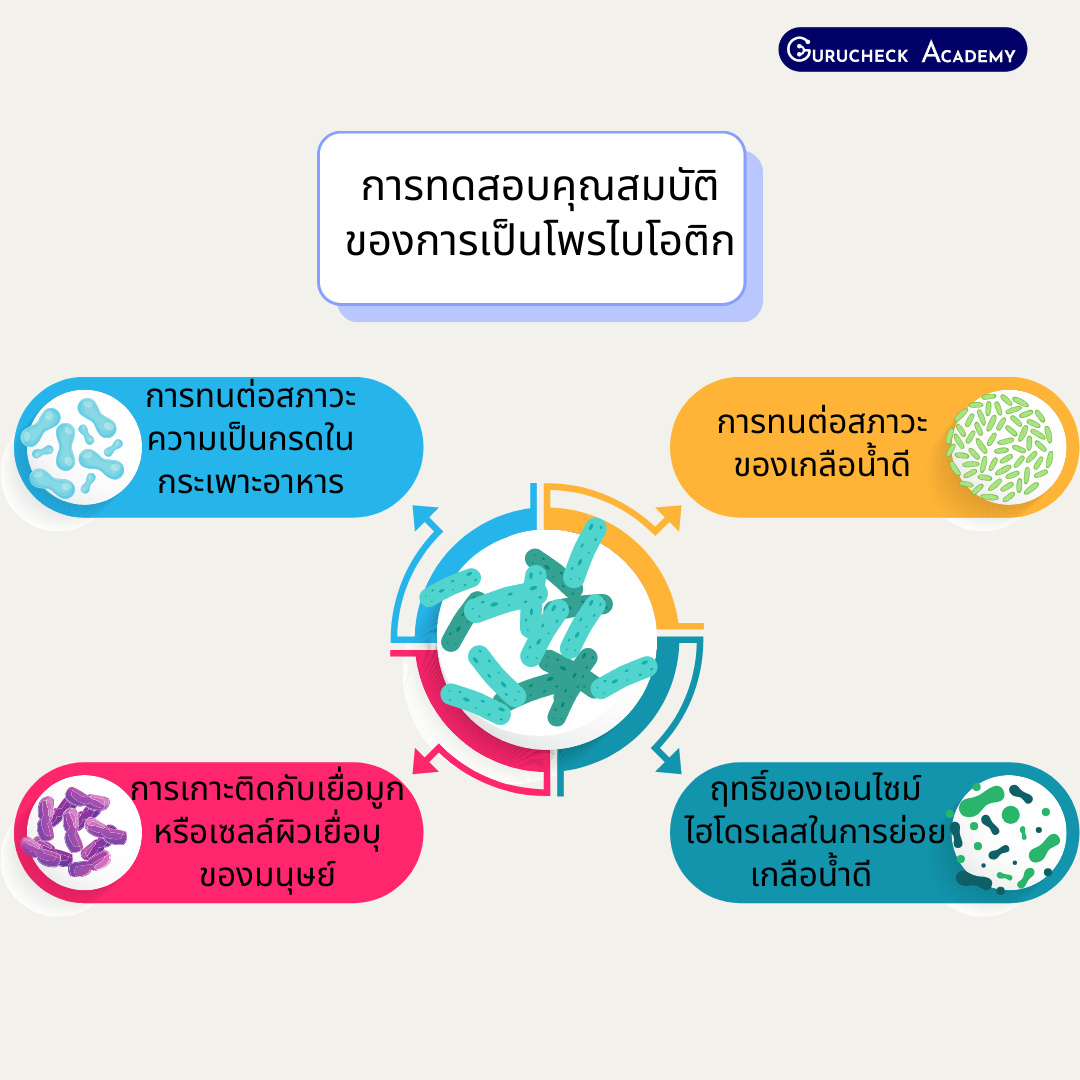
การทดสอบคุณสมบัติของการเป็นโพรไบโอติกมีดังนี้
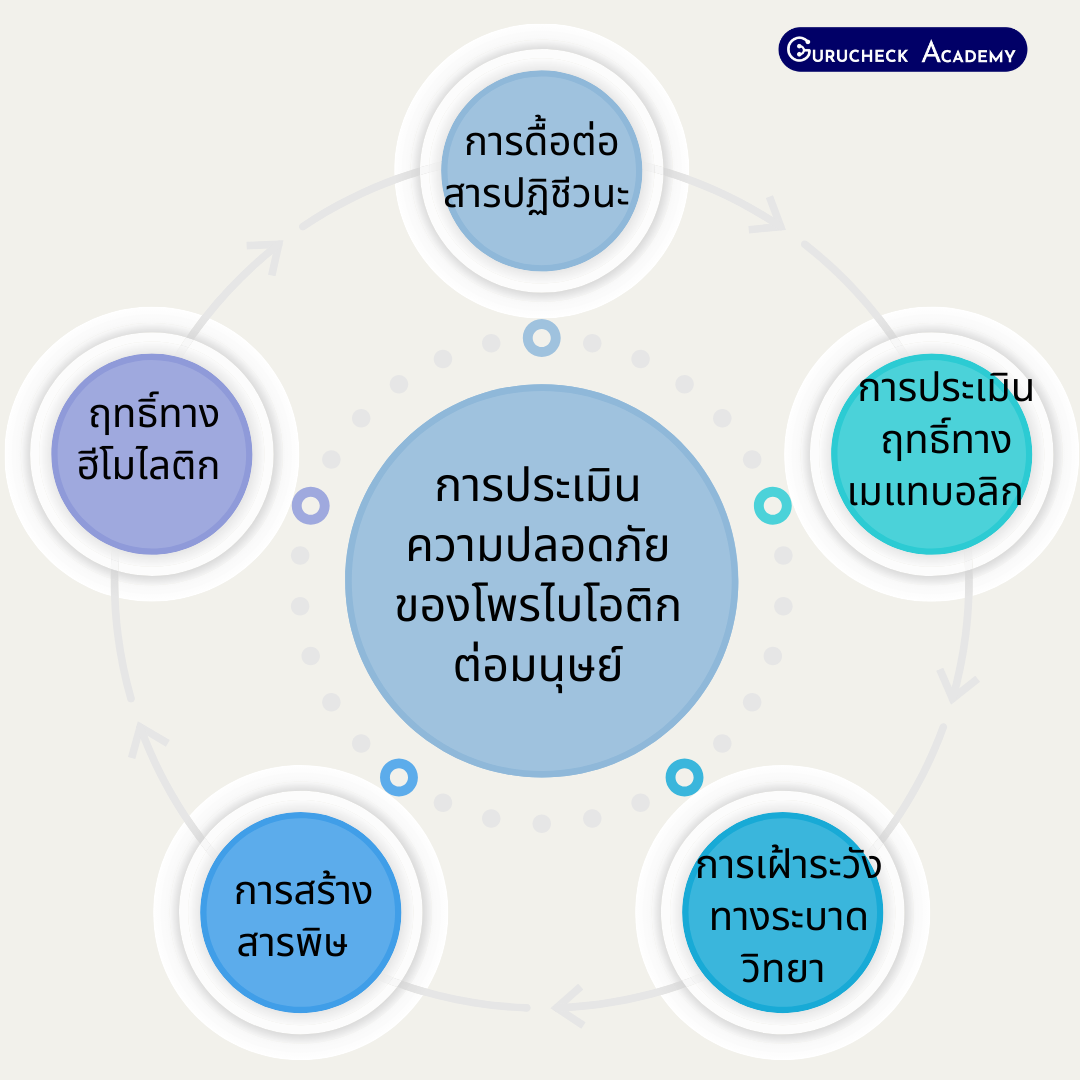
โดยการทดสอบในหลอดทดลอง (in vitro) หรือในสัตว์ทดลอง (in vivo) และการศึกษาในมนุษย์เพื่อประเมินความปลอดภัย และ ปฏิกิริยาของร่างกายต่อโพรไบโอติก ดังนี้
- การดื้อต่อสารปฏิชีวนะ โดยทดสอบทั้งลักษณะการแสดงออก (phenotype) และลักษณะทางพันธุกรรม (genotype) ซึ่งการทดสอบ phenotype จะทดสอบค่าความเข้มข้นต่ำสุดของสารปฏิชีวนะที่สามารถยับยั้งการเจริญเติบโตของจุลินทรีย์ได้ (minimum inhibitory concentration: MIC) โดยใช้วิธี microdilution method ตามมาตรฐานสากล เช่น CLSI หรือ ISO ที่จำเพาะกับจุลินทรีย์ชนิด (species) นั้น ๆ ส่วนการทดสอบทาง genotype จะวิเคราะห์หายีนดื้อต่อสารปฏิชีวนะโดยใช้ข้อมูล WGS และค้นหายีนด้วยฐานข้อมูลที่เหมาะสมและเป็นปัจจุบันอย่างน้อย 2 แห่ง โดยฐานข้อมูลที่ใช้1 แห่ง คือ Kyoto Encyclopedia of Genes and Genomes (KEGG) ทั้งนี้ข้อมูลที่ค้นหาต้องไม่เกิน 2 ปี ณ วันที่ยื่นประเมิน
- การประเมินฤทธิ์ทางเมแทบอลิก เช่น การผลิตดี-แลกเทต (D-lactate) หรือการสลายเกลือน้ำดีเป็นต้น โดยระบุวิธีการ สภาวะ ผล และสรุปผล โดยวิธีการที่เหมาะสมการประเมินผลข้างเคียงระหว่างการศึกษาในมนุษย์ โดยระบุวิธีการ สภาวะ และผลข้างเคียงที่เกิดขึ้นหรือใช้ข้อมูลการทบทวนวรรณกรรมอย่างเป็นระบบ (systematic review) จากหน่วยงานหรือองค์กรที่มีระบบประเมินความปลอดภัยที่น่าเชื่อถือก็ได้
- การเฝ้าระวังทางระบาดวิทยาของอุบัติการณ์ที่ไม่พึงประสงค์ ในกรณีออกวางจำหน่ายแล้วในท้องตลาดต้องเฝ้าระวังลูกค้า แต่ในกรณีที่ยังไม่วางจำหน่าย ให้ระบุแผนการเฝ้าระวัง และวิธีการเก็บข้อมูลหลังการออกจำหน่าย
- การสร้างสารพิษ กรณีที่สายพันธุ์ที่ประเมินนั้นเป็นจุลินทรีย์ชนิดที่มีการผลิตสารพิษ วิเคราะห์ความสามารถในการสร้างสารพิษและหรือสารไม่พึงประสงค์ โดยอาจใช้การวิเคราะห์ข้อมูล WGS (in silico) การทดสอบ cytotoxicity ในเซลล์ไลน์ (in vitro) หรือในสัตว์ทดลอง (in vivo)
- ฤทธิ์ทางฮีโมไลติก กรณีที่สายพันธุ์ที่ประเมินนั้นอยู่ในกลุ่มของจุลินทรีย์ ชนิดที่มีโอกาสทำให้เกิดการแตกของเม็ดเลือดแดง ทดสอบฤทธิ์ทางฮีโมไลติก โดยระบุวิธีทดสอบ ชนิดหรือแหล่งที่มาของเลือดที่ใช้ในการทดสอบ และผลการทดสอบ

ขั้นตอนการขอใช้โพรไบโอติกสายพันธุ์อื่นนอกเหนือจากที่กำหนดไว้
ผู้ผลิตหรือนำเข้าโพรไบโอติกสายพันธุ์ใหม่ ที่ยังไม่มีประกาศใช้ได้ในทย จะต้องมีการดำเนินตามขั้นตอนต่างๆ ตามที่กูรูเช็คได้นำเสนอไป เพื่อประกาศให้สามารถใช้โพรไบโอติกในอาหารหรืออาหารเสริมได้ โดยผ่านการตรวจสอบ การรับรอง หลายขั้นตอน ขอให้ผู้ผลิตหรือนำเข้าศึกษาข้อมูลให้ละเอียด หรือติดต่อสอบถามข้อมูลเพิ่มเติมที่กองอาหาร กระทรวงสาธารณสุข โทรศัพท์ 0-2590-7185, 0-2590-7179 ซึ่งจะสิ้นสุดการส่งข้อมูลภายในวันที่ 30 เมษายน 2567 นี้นะคะ

ปรึกษาพัฒนาสูตรกับผู้เชี่ยวชาญเภสัชกร R&D

(ติดต่อเรา)
“กูรูเช็คสร้างชุมชนสำหรับเจ้าของเเบรนด์ และโรงงาน OEM จากความต้องการจริงของตลาดอาหารเสริม สกินเเคร์ และผู้บริโภค ด้วยประสบการณ์ตรงในการเป็นผู้รีวิว เราจึงตั้งใจเป็นที่ปรึกษา พัฒนาสูตร(NPD)ให้กับเจ้าของเเบรนด์ เเละเป็นแพลตฟอร์มที่รวมโรงงาน OEM ที่มีความเก่งในเเต่ละด้านไว้ ให้ตอบโจทย์การผลิตอาหารเสริม สกินเเคร์ ที่ออกฤทธิ์ได้จริงตามงานวิจัย ซึ่งเป็นนโยบายหลักของเรา เพื่อยกระดับวงการอาหารเสริม สกินเเคร์ของไทยให้เเข่งขันได้ในระดับสากล“